Banyuls-sur-Mer (Côte Vermeille, nord-ouest Méditerranée), au sein du Parc naturel marin du golfe du Lion, est depuis longtemps reconnue comme un site majeur de biodiversité marine. Ce statut doit autant à la mosaïque d’habitats côtiers qu’à une tradition scientifique exceptionnelle portée par le Laboratoire Arago, renforcée par la création de la Réserve naturelle nationale marine de Cerbère-Banyuls en 1974. À l’échelle régionale, la Méditerranée apparaît en outre comme un système où certains territoires insulaires et secteurs protégés pourraient jouer un rôle de refuges pour des espèces menacées, notamment chez les élasmobranches, renforçant l’intérêt d’inventaires non invasifs et comparables dans le temps [1]. Pourtant, sur cette côte abrupte où le plateau bascule rapidement vers le large, une part importante de la biodiversité reste étonnamment mal connue : celle des canyons de profondeur.
Ce déficit de connaissance est avant tout un problème d’accessibilité. Les inventaires reposent encore largement sur des méthodes traditionnelles (plongée, imagerie, captures), mais celles-ci deviennent vite inopérantes lorsque la profondeur augmente. Les habitats profonds sont hors de portée de la plongée, et les reliefs accidentés des canyons rendent l’usage d’engins de pêche difficile, risqué, voire incompatible avec les objectifs de conservation ; à cela s’ajoutent des contraintes réglementaires dans et autour des aires protégées qui limitent les approches extractives. Or ces écosystèmes profonds, d’une importance fonctionnelle disproportionnée, figurent toujours parmi les plus sous-échantillonnés à l’échelle mondiale [2–4]. Autrement dit, une fraction de la biodiversité locale est située dans un espace que l’on n’échantillonne que rarement — et rarement bien.
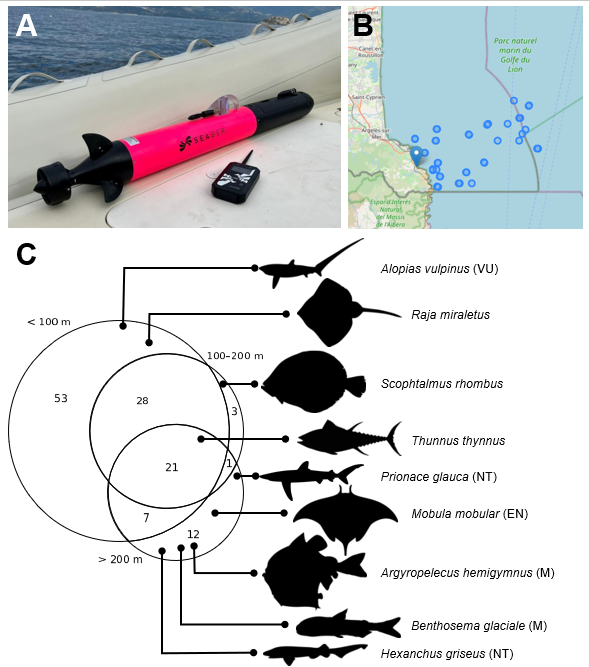
Ici, un véhicule sous-marin autonome (Fig. 1A) équipé d’un collecteur d’ADN environnemental (ADNe) a été déployé afin d’inventorier l’ichtyofaune le long d’un gradient bathymétrique jusqu’à 300 m au large de Banyuls (Figure 1B). L’ADNe correspond à l’ADN extrait directement d’échantillons environnementaux (par exemple, eau, sol ou sédiments), sans isolement préalable des organismes, et permet d’identifier les espèces présentes, y compris celles rares ou difficiles à détecter [5–7]. Si l’ADNe s’est imposé comme un outil majeur du suivi de la biodiversité et de la conservation [6–8], il a également démontré sa capacité unique à révéler la diversité de groupes historiquement difficiles à inventorier, comme les requins [9]. Pourtant, l’ADNe reste encore rarement appliqué de façon réellement intégrative dans les environnements profonds et structurés, là où les approches traditionnelles échouent. En embarquant une tête préleveuse d’ADNe sur un robot capable d’échantillonner des milieux complexes, profonds et parfois réglementés, nous testons une stratégie opérationnelle pour explorer ces habitats sans captures, et sans dommage pour des écosystèmes potentiellement vulnérables.
Campagne de terrain & méthodes
Du 4 au 17 septembre 2025, nous avons réalisé 23 transects AUV d’environ 2 km au large de Banyuls, couvrant un gradient bathymétrique (≈35–300 m). Chaque transect a été parcouru par deux AUV à quelques minutes d’intervalle, fournissant deux réplicas indépendants. L’eau de mer a été filtrée in situ via un module de filtration1 embarqué dans la tête de l’AUV, intégrant un filtre haute capacité (filtration minimale 30 L). En complément, trois transects de surface ont été réalisés comme contrôle (pompe péristaltique, deux réplicas par transect) afin de comparer le signal ADNe de surface à celui obtenu par collecte AUV. Les filtres ont été conservés dans une solution tampon puis traités en laboratoire.
L’ADN a été extrait, amplifié à l’aide d’un couple d’amorces universel poissons (teleo [10]) ciblant une portion du gène mitochondrial 12S et séquencé grâce à la technologie haut débit d’Illumina®. Les séquences obtenues ont été traitées avec un pipeline bioinformatique optimisé pour l’analyse de l’ADNe et comparées avec une base de référence locale comprenant plus de 70 % des espèces de poissons de Méditerranée. Les « groupes d’espèces » correspondant à une assignation ambiguë ont été traités comme un taxon unique, tandis que les read counts ont été interprétés comme un proxy d’intensité du signal ADNe [11,12].
106 espèces ont été détectées le long des transects de surface, tandis que 125 espèces ont été observées dans les transects AUV en profondeur, avec seulement 61 espèces communes aux deux approches. Les transects réalisés à l’aide d’AUV apportent ainsi une information complémentaire aux transects de surface, cohérente avec l’accès à des habitats profonds généralement absents des inventaires classiques. La robustesse de l’approche est renforcée par la comparaison des réplicas AUV : les deux passages partagent une fraction importante des détections mais restent fortement complémentaires (indice de Jaccard moyen 0,43 ± 0,16), indiquant qu’un seul passage manquerait une part non négligeable de la diversité — en particulier des espèces rares, très mobiles ou faiblement détectables. Cette complémentarité justifie la réplication comme stratégie simple et efficace pour améliorer l’exhaustivité, un point crucial dans des milieux hétérogènes et fragmentés comme les pentes et canyons.
Dans les échantillons prélevés par AUV entre 35 et 300 m, les espèces détectées présentent une structuration bathymétrique marquée : 109 espèces à moins de 100 mètres de profondeur, 53 espèces entre 100 et 200 mètres, et 41 espèces à plus de 200 mètres. Le turnover est élevé, avec 53 espèces limitées aux faibles profondeurs, 12 espèces strictement profondes (>200 m) et seulement 21 espèces présentes sur l’ensemble du gradient bathymétrique (Figure 1C).
Les transects réalisés par AUV révèlent ainsi un compartiment profond distinct, plutôt qu’une simple extension atténuée de la biodiversité côtière. Cet apport est particulièrement notable pour la composante offshore profonde, incluant une faune mésopélagique rarement documentée à l’échelle locale. À des profondeurs >200 m, nous détectons de manière récurrente des espèces emblématiques du mésopélagique, telles que des poissons lanternes (Benthosema glaciale, Diaphus holti, Ceratoscopelus maderensis, Lampanyctus crocodilus, Myctophum punctatum), mais aussi des poissons hachettes (Argyropelecus hemigymnus) et des poissons dragons (Chauliodus sloani, Stomias boa). La détection de ces taxons à ces profondeurs est cohérente avec la capture d’un signal proche de la limite supérieure de leurs migrations verticales nocturnes, un processus clé de l’écologie mésopélagique [13,14]. En d’autres termes, l’AUV collecteur d’ADNe rend lisible un compartiment historiquement sous-échantillonné, jusque-là largement invisible.

Au-delà de la composition spécifique, les proxys semi-quantitatifs (nombre de séquences d’ADN obtenues combinés au nombre de réplicas positifs) confirment cette structuration. Malgré les limites connues des read counts (variations de relargage, transport, amplification), les profils dominants sont remarquablement cohérents entre réplicats et transects. Les faibles profondeurs présentent des signatures fortes et répétées d’espèces néritiques abondantes et/ou à forte production d’ADNe (p. ex. Pagellus acarne, Sardina pilchardus, Sardinella aurita, Engraulis encrasicolus), alors qu’au-delà de 200 m, la dominance du signal bascule vers des taxons mésopélagiques. La zone 100–200 m apparaît ainsi comme une interface où coexistent signaux côtiers persistants et renforcement de taxons du plateau externe. Cette concordance entre structuration taxonomique et structuration des signaux dominants renforce l’interprétation d’un compartiment profond fonctionnellement distinct.
Chondrichthyens : détecter l’invisible
Nous détectons également une diversité non négligeable de poissons cartilagineux, groupe emblématique des limites des approches classiques. Au total, 13 espèces de Chondrichthyens (requins/raies) sont détectées sur 125 espèces, soit 10,4 % des espèces inventoriées — un résultat cohérent avec l’idée que l’ADNe met en lumière une part significative de diversité souvent manquée chez les requins [9]. De manière remarquable, huit de ces espèces à enjeu de conservation n’ont pas été détectées dans les transects de surface, ce qui souligne le gain d’information fourni par l’accès robotisé au profond. Ces espèces incluent des taxons benthiques et/ou associés à des fonds plus profonds, pour lesquels le signal ADNe est fortement structuré par la profondeur en Méditerranée [15,17]. Parmi ces espèces figurent Dasyatis marmorata (NT), Mustelus asterias (NT) et Raja asterias (NT). S’y ajoutent des espèces très mobiles comme Alopias vulpinus (VU), Mobula mobular (EN) et Prionace glauca (NT), ainsi qu’un taxon particulièrement élusif, le requin griset Hexanchus griseus (NT).

Cette capacité à révéler et suivre des Chondrichthyens menacés est d’autant plus critique que ce groupe concentre une part majeure du risque d’érosion de l’histoire évolutive marine [18].
Conclusion
Ces observations soulignent un point simple mais central : les écosystèmes profonds jouent un rôle fonctionnel majeur (flux de matière, connectivité trophique, couplage côte-large), mais restent paradoxalement parmi les moins observés et les moins compris — principalement parce qu’ils sont difficiles d’accès. Dans des environnements complexes comme les canyons et pentes externes, où la plongée, le chalutage ou certaines approches instrumentées sont impraticables, inadaptées ou limitées par des contraintes réglementaires, un AUV collecteur d’ADNe propose une alternative : explorer sans dégrader, inventorier sans capturer, et rendre visibles des communautés longtemps hors de portée. Au large de Banyuls, cette approche transforme une frontière historique de l’échantillonnage en un espace de connaissance. Elle suggère surtout une idée générale : les « zones blanches » de la biodiversité marine ne sont pas forcément pauvres — elles sont souvent seulement inaccessibles [2–4].
En les rendant observables, ce système autonome d’échantillonnage sous-marin ouvre un champ nouveau pour comprendre et suivre des écosystèmes profonds dont l’importance est reconnue, mais dont la biodiversité reste encore largement à découvrir. Cette approche se révèle particulièrement pertinente dans le contexte du suivi de la biodiversité au sein d’aires marines protégées.
Références
- Pichot, F., Mouillot, D., Juhel, J.B., et al. (2025). Mediterranean islands as refugia for elasmobranch and threatened fishes. Diversity and Distributions 31(2), e13937.
- Danovaro, R., Company, J.B., Corinaldesi, C., et al. (2010). Deep-sea biodiversity in the Mediterranean Sea: the known, the unknown, and the unknowable. PLoS ONE 5, e11832.
- Puig, P., Canals, M., Company, J.B., et al. (2014). Submarine canyons and their role in deep-sea biodiversity and transport processes. Progress in Oceanography 128, 1–12.
- Ramirez-Llodra, E., Brandt, A., Danovaro, R., et al. (2010). Deep, diverse and definitely different: unique attributes of the world’s largest ecosystem. Biogeosciences 7, 2851–2899.
- Taberlet, P., Coissac, E., Hajibabaei, M., & Rieseberg, L.H. (2012). Environmental DNA. Molecular Ecology 21, 1789–1793.
- Valentini, A., Taberlet, P., Miaud, C., et al. (2016). Next-generation monitoring of aquatic biodiversity using eDNA metabarcoding. Molecular Ecology 25, 929–942.
- Thomsen, P.F., & Willerslev, E. (2015). Environmental DNA — an emerging tool in conservation for monitoring past and present biodiversity. Biological Conservation 183, 4–18.
- Deiner, K., Bik, H.M., Mächler, E., et al. (2017). Environmental DNA metabarcoding: Transforming how we survey animal and plant communities. Molecular Ecology 26, 5872–5895.
- Boussarie, G., Bakker, J., Wangensteen, O.S., et al. (2018). Environmental DNA illuminates the dark diversity of sharks. Science Advances 4(5), eaap9661.
- Valentini, A., Taberlet, P., Miaud, C., et al. (2016). Next-generation monitoring of aquatic biodiversity using eDNA metabarcoding. Mol. Ecol. 25, 929–942.
- Barnes, M.A., & Turner, C.R. (2016). The ecology of environmental DNA and implications for conservation genetics. Conservation Genetics 17, 1–17.
- Rozanski, R., Velez, L., Hocdé, R., et al. (2024). Seasonal dynamics of Mediterranean fish communities revealed by eDNA. Ecological Indicators 166, 112290.
- Robinson, C., Steinberg, D.K., Anderson, T.R., et al. (2010). Mesopelagic zone ecology and biogeochemistry — a synthesis. Biogeosciences 7, 3419–3436.
- Brierley, A.S. (2014). Diel vertical migration. Current Biology 24, R1074–R1076.
- Rozanski, R., et al. (2024). Seasonal dynamics of Mediterranean fish communities revealed by eDNA. Ecological Indicators 166, 112290.
- Mission BioDivMed (2024). Guide d’utilisation de l’ADNe en milieu marin : connaître, comprendre et utiliser l’ADNe pour préserver la biodiversité marine. Document technique.
- Ministère de la Transition écologique (2024). Mission BioDivMed 2023 : une cartographie inédite de la biodiversité marine méditerranéenne grâce à l’ADN environnemental (ADNe).
- Stein, R.W., Mull, C.G., Kuhn, T.S., et al. (2018). Global priorities for conserving the evolutionary history of sharks, rays and chimaeras. Nature Ecology & Evolution 2, 288–298.
- Dalongeville, A., Boulanger, E., Marques, V., et al. (2022). Benchmarking eleven biodiversity indicators based on environmental DNA surveys. Journal of Applied Ecology 59(11), 2803–2813.
- Mathon, L., Marques, V., Mouillot, D., et al. (2022). Cross-ocean patterns in fish biodiversity on coral reefs through the lens of eDNA metabarcoding. Proceedings of the Royal Society B 289(1973).